A ciência das células-tronco está avançando. Como destaquei acima, estamos vendo alguns ensaios clínicos incrivelmente promissores. Mas, até 2019, além do sangue do cordão umbilical, não vimos nenhuma terapia de células-tronco aprovada no mercado dos EUA.
Curiosamente, esse vazio no mercado está sendo preenchido com clínicas de células-tronco quase-legais, realizando procedimentos não aprovados pela FDA com terapias questionáveis.
Na década passada, se você desejasse uma terapia com células-tronco, precisaria se envolver em turismo de células-tronco. O turismo de células-tronco implicava viagens internacionais para a China, México, Índia, Panamá, etc. em busca de um médico que oferecesse tratamento com células-tronco. Atualmente, esse esforço internacional não é mais necessário. Uma pesquisa recente identificou 570 clínicas nos Estados Unidos atualmente vendendo terapias com células-tronco diretamente aos consumidores.
O que essas clínicas de células-tronco estão vendendo?
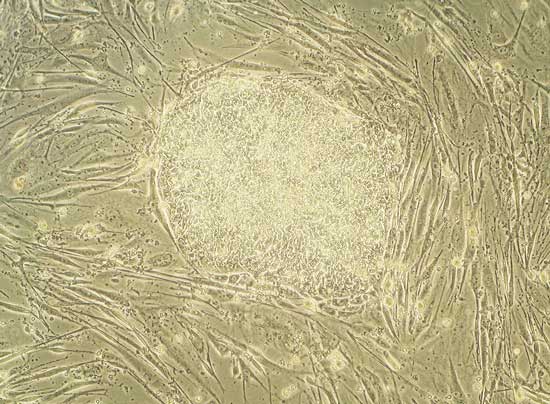
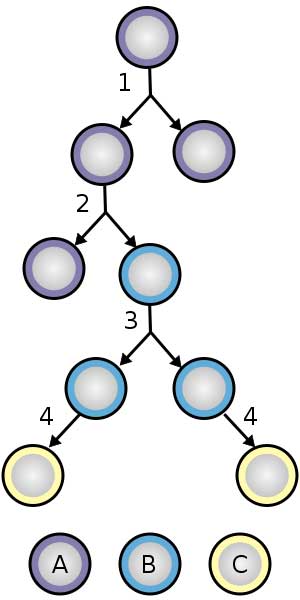
A maioria dessas clínicas está vendendo tratamentos autólogos. Como mencionado anteriormente, um tratamento autólogo envolve a remoção de células-tronco de uma parte do corpo, o processamento dessas células de alguma forma e o transplante de volta para o mesmo indivíduo. Muitas clínicas estão extraindo gordura e isolando as células-tronco adiposas do tecido adiposo. Nosso tecido adiposo é uma fonte rica de células-tronco. O termo técnico para as células-tronco em nossa gordura são as células-tronco adiposas. De acordo com esse relatório de 2016, 61% dos tratamentos oferecidos pelas clínicas de células-tronco dos EUA são tratamentos com células-tronco adiposas. Outros tratamentos comumente realizados utilizam as células-tronco hematopoéticas encontradas na medula óssea. OK, então as clínicas estão usando principalmente células-tronco da gordura ou da medula óssea …
Quais doenças são tratadas por essas clínicas?
O principal serviço oferecido por essas clínicas é o tratamento de doenças ortopédicas. Essas terapias ortopédicas geralmente envolvem o uso de células-tronco para reduzir problemas nas articulações ou nos tecidos moles. As clínicas afirmam que seus tratamentos ortopédicos com células-tronco podem reduzir a dor e a inflamação. Essas afirmações podem ser verdadeiras ou podem não ser verdadeiras. A ciência ainda é inconclusiva. Clínicas menos escrupulosas prometem antienvelhecimento, aumento do pênis ou tratamento para Parkinson, Esclerose Múltipla, Paralisia Cerebral e danos na medula espinhal. Isto é o que acontece em um ambiente não regulamentado, nada está fora da mesa.
A verdade é que certas injeções de células-tronco podem ser apropriadas para uma ampla gama de doenças, mas cientistas profissionais ainda estão trabalhando para determinar a segurança e a eficácia dos procedimentos.
Ainda não temos certeza de que tipos de células irão se desenvolver a partir das células-tronco, uma vez que elas são transplantadas para certas partes do corpo. Essas células-tronco transplantadas podem formar um tumor cancerígeno … ou um sério problema de rejeição imunológica …
Um consumidor prudente esperaria até que as dúvidas fossem eliminadas.
Por que a FDA não está reprimindo essas clínicas de células-tronco não aprovadas?
Essa é a verdadeira questão. Não é de surpreender que uma comunidade empresarial agressiva e ágil esteja se esforçando para ganhar dinheiro em nome de células-tronco. Isso é o que os mercenários fazem … eles correm. Alguns clientes estão pagando 15K, do bolso, por procedimentos com células-tronco. Quando há demanda, haverá oferta.
No entanto, é surpreendente que o FDA esteja passivamente permitindo que o nicho se desenvolva.
Em novembro de 2017, o FDA divulgou uma Orientação da Indústria revisada sobre clínicas de células-tronco. Essa orientação reforça a definição do que é permitido nessas clínicas. Em essência, o FDA permite que o tecido biológico seja usado apenas na parte do corpo da qual o tecido foi extraído. Além disso, o FDA permite apenas a manipulação mínima do tecido do paciente. Se uma clínica está agindo fora desses parâmetros, ela está vendendo um medicamento e exigirá o licenciamento apropriado.
Por exemplo, não é legal para uma clínica remover o tecido adiposo da coxa de um paciente, isolar as células-tronco adiposas e depois injetar essas células-tronco no cotovelo de uma pessoa com dor nas articulações. Esse procedimento envolve mais do que o processamento mínimo e muda o tecido biológico do local A para o local B. Portanto, esse procedimento é uma violação da nova Orientação da Indústria do FDA.
Ok… mas aqui está a estranha notícia. O FDA está fornecendo a essas clínicas 36 meses para cumprir os regulamentos mais rigorosos. Para aqueles que seguem em casa, 36 meses são três anos. Muitos tratamentos imprudentes e caros podem ser realizados em 3 anos.
Três anos é muito tempo para que clínicas potencialmente não-conformes continuem ganhando massa de pacientes.–Paul Knoepfler
Então, o que o FDA faz?
A resposta curta é. . . Eu não sei exatamente.
Eu ouvi um representante da FDA falar sobre esse assunto em um simpósio médico no final de 2018. O palestrante explicou que o FDA simplesmente não tem orçamento e pessoal suficientes para investigar e responder ao enorme volume de clínicas semi-legais de células-tronco.
No entanto, ao fornecer 3 anos para as clínicas se regulamentarem, o FDA está endossando tacitamente a experimentação humana com vários tratamentos com células-tronco. Talvez o FDA veja esse período de carência como uma oportunidade para deixar o mercado definir quais tratamentos oferecem o melhor valor.
Além disso, muitos desses tratamentos com células-tronco estão ampliando a definição de um medicamento. Se você remover células-tronco do seu corpo, centrifugar as células, tratá-las em um laboratório e depois injetá-las de volta em seu próprio corpo … isso é realmente uma droga biológica? Talvez o FDA esteja em dúvida em termos da melhor forma de categorizar esses tratamentos? Novamente, três anos assistindo essas clínicas operarem poderia ajudar a tomar essa decisão regulatória.
Também deve ser mencionado que, além de emitir novas orientações, o comissário do FDA (Scott Gottlieb) está indo atrás dos criminosos mais notórios no universo de células-tronco. Por exemplo, a FDA enviou uma carta de alerta severa para a Stem Cell Clinic, uma organização localizada em Sunrise, Flórida. Essa clínica particular supostamente injetou células-tronco nos globos oculares de três mulheres idosas. Essas mulheres estavam buscando alívio da degeneração macular. De acordo com o New England Journal of Medicine, o tratamento com células-tronco falhou e levou à cegueira nessas mulheres.
A perda visual grave dos pacientes após a injeção foi associada à hipertensão ocular, retinopatia hemorrágica, hemorragia vítrea, tração combinada e descolamento de retina regmatogênico ou luxação do cristalino.
Palavra para o sábio, quando se envolver em tratamentos experimentais e não comprovados…. mantê-lo fora de seus globos oculares.
Com toda a seriedade, se você está considerando um produto de terapia com células-tronco não aprovado pelo FDA,o FDA emitiu recomendações para ajudar a orientar a decisão do consumidor. Pergunte à clínica se o FDA emitiu um INDA (Investigational New Drug Application) para o tratamento. A presença de um INDA sinaliza que o FDA, pelo menos, começou a rever o tratamento. Se a clínica fornecer um número INDA, você poderá revisar as informações públicas por conta própria ou com seu médico. Se você estiver participando de uma terapia com células-tronco como participante de um ensaio clínico, solicite o folheto do pesquisador clínico. Essa brochura inclui informações sobre segurança e eficácia.
Conclusão…
- Clínicas de células-tronco agora estão localizadas por todo os EUA.
- A maioria dessas clínicas está operando fora dos regulamentos do FDA. Eles estão fazendo muito mais do que o processamento mínimo de tecido biológico antes do transplante. Eles também estão transplantando as células-tronco processadas em locais diferentes da área onde o tecido foi removido. Ambas as ações tornam o tratamento ilegítimo pelos regulamentos atuais do FDA.
- Na maior parte, o FDA está esperando três anos para começar a aplicar essas novas regulamentações.
Continuarei atualizando esta página à medida que o campo da ciência das células-tronco evoluir.
Continua…